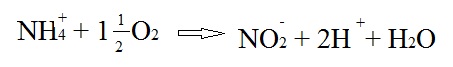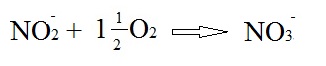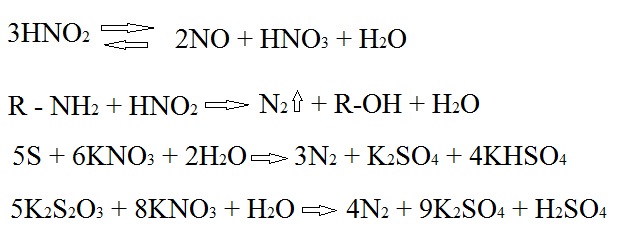Nitrifikatsioon
Ammoniaak, mis moodustus orgaanilise aine lagunemisel mullas, sõnnikus, vees jne., oksüdeeritakse kiiresti nitrititeks ja nitraadiks. Seda protsessi nimetatakse nirtifikatsiooniks.
Kuni 19. Sajandi keskpaigani arvati, et NH3 oksüdatsioon on keemiline reaktsioon, milles mullal on katalüsaatori osa. 1877. a tõestati eksperimentaalselt, et nitrifikatsiooni kutsuvad esile mullas mikroorganismid. 1 m pikkusest kvartsklaasist torust lasti läbi reovett. Torud olid täidetud liiva ja aiamulla seguga. Üks torudest oli kuumutatud ja selle sisaldisele lisatud antiseptikuid, teine lisanditeta ja kuumutamata. Reovee filtratsioonil panid uurijad tähele, et kuumutamata torus vähenes ammoniakaalse lämmastiku sisaldus ja suurenes nitraatide sisaldus. Toru kuumutamisel ja antiseptikute lisamisel ammoniaagi oksüdatsiooni praktiliselt ei toimunud. Uurijatel ei õnnestunud eraldada nitrifikatsiooni põhjustavaid baktereid, kuna nad kasutasid mikroobide kasvatamisel puljongsöödet.
1890. a. selgitati Vinogratski poolt nitrifikatsiooni bioloogiline olemus. Ta näitas, et nitrifikaatorid ei kasva söötmetel, mis sisaldavad orgaanilisi aineid. Nitrifikaatorid osutusid autotroofseteks, seega väga tundlikeks orgaanilistele ühenditele söötmetes. Nitrifikaatoreid õnnestus eraldada, kui kasutati mineraalseid söötmeid. Võeti kasutusele ränihappe baasil valmistatud söötmed, kuhu lisati ammooniumsoolasid. Selgus, et rida mikroorganisme saavad rakuainete sünteesiks energiat NH3 oksüdatsioonisl nitrititeks ja teised jälle nitritite oksüdatsioonil nitraatides. Esimeses etapis osalevad nirosobakterid: Nitrosomonase spp., Nitrospira spp., ja Nitrosocuccus`e spp., Nitrosovobrio spp., Nitrosolobus spp. jt.
Nitrifikatsiooni I faasi võiks kirjeldada järgmiselt:
Kuni 19. Sajandi keskpaigani arvati, et NH3 oksüdatsioon on keemiline reaktsioon, milles mullal on katalüsaatori osa. 1877. a tõestati eksperimentaalselt, et nitrifikatsiooni kutsuvad esile mullas mikroorganismid. 1 m pikkusest kvartsklaasist torust lasti läbi reovett. Torud olid täidetud liiva ja aiamulla seguga. Üks torudest oli kuumutatud ja selle sisaldisele lisatud antiseptikuid, teine lisanditeta ja kuumutamata. Reovee filtratsioonil panid uurijad tähele, et kuumutamata torus vähenes ammoniakaalse lämmastiku sisaldus ja suurenes nitraatide sisaldus. Toru kuumutamisel ja antiseptikute lisamisel ammoniaagi oksüdatsiooni praktiliselt ei toimunud. Uurijatel ei õnnestunud eraldada nitrifikatsiooni põhjustavaid baktereid, kuna nad kasutasid mikroobide kasvatamisel puljongsöödet.
1890. a. selgitati Vinogratski poolt nitrifikatsiooni bioloogiline olemus. Ta näitas, et nitrifikaatorid ei kasva söötmetel, mis sisaldavad orgaanilisi aineid. Nitrifikaatorid osutusid autotroofseteks, seega väga tundlikeks orgaanilistele ühenditele söötmetes. Nitrifikaatoreid õnnestus eraldada, kui kasutati mineraalseid söötmeid. Võeti kasutusele ränihappe baasil valmistatud söötmed, kuhu lisati ammooniumsoolasid. Selgus, et rida mikroorganisme saavad rakuainete sünteesiks energiat NH3 oksüdatsioonisl nitrititeks ja teised jälle nitritite oksüdatsioonil nitraatides. Esimeses etapis osalevad nirosobakterid: Nitrosomonase spp., Nitrospira spp., ja Nitrosocuccus`e spp., Nitrosovobrio spp., Nitrosolobus spp. jt.
Nitrifikatsiooni I faasi võiks kirjeldada järgmiselt:
Nitrifikatsiooni II faasis osalevad nitrobakterid nagu Nitrobacter winogradskii, Nitrobacter agilis jt. Nitrifikatsiooni II faasi võiks kirjeldada järgnevalt:
Nitrifikatsiooni etapilisust iseloomustab metabioosi nähtus. See iseloomustab mikroorganismide sellist vastastikust suhet, mul üks mikroorganism areneb pärast teist, kasutades esimese elutegevuse produkte. NH3 oli valgulagundajate ainevahetussaadus, mida kasutavad nirosobakterid produtseerides nitriteid, mida omakorda kasutavad nitrobakterid oma elutegevusel.
Nirtifikatsiooni toimumise eeldused:
1. Keskkonnas peab olema ammoniaaki (NH3). Seega nirtifikatsioon toimub intensiivselt näiteks reovees, kompostis, sõnnikus jne.
2. Keskkonnas peab olema tagatud piisav hapniku (O2) juurdepääs ja ta peab olema mõõduka happelise reaktsiooniga(pH väärtusel alla 5 reaktsioon lakkab).
3. Soodustavates teguriteks happelisemates muldades on nende lupjamine lupjamine, õhustamine ja liigniiskuse all kannatavate muldade põhjavee seisu alandamine.
Kultuuristamata muldadel, kus lämmastiku allikaks on lehekõdu, oksad jne, toimub protsess halva õhustatuse tõttu aeglasemalt.. Metsamassiivid saavad lämmastikku kõdunevast orgaanilisest ainest ja õhulämmastikku siduvate mikroobide poolt.
Denitrifikatsioon
Keskkonnas (nt vees, mullas jt.) toimub rida protsesse, kus lämmastiku oksüdeerunud vormid võidakse järk-järgult taandada kuni molekulaarse õhulämmastikuni. Selle tulemusel tekib taimedele vajalike lämmastikühendite kadu.
Tugevalt happelistes muldades, kus pH väärtus on alla 5,5 toimub enamasti ainult keemiline reaktsioon – oksüdeerunud lämmastikühendite taandamine.
Nirtifikatsiooni toimumise eeldused:
1. Keskkonnas peab olema ammoniaaki (NH3). Seega nirtifikatsioon toimub intensiivselt näiteks reovees, kompostis, sõnnikus jne.
2. Keskkonnas peab olema tagatud piisav hapniku (O2) juurdepääs ja ta peab olema mõõduka happelise reaktsiooniga(pH väärtusel alla 5 reaktsioon lakkab).
3. Soodustavates teguriteks happelisemates muldades on nende lupjamine lupjamine, õhustamine ja liigniiskuse all kannatavate muldade põhjavee seisu alandamine.
Kultuuristamata muldadel, kus lämmastiku allikaks on lehekõdu, oksad jne, toimub protsess halva õhustatuse tõttu aeglasemalt.. Metsamassiivid saavad lämmastikku kõdunevast orgaanilisest ainest ja õhulämmastikku siduvate mikroobide poolt.
Denitrifikatsioon
Keskkonnas (nt vees, mullas jt.) toimub rida protsesse, kus lämmastiku oksüdeerunud vormid võidakse järk-järgult taandada kuni molekulaarse õhulämmastikuni. Selle tulemusel tekib taimedele vajalike lämmastikühendite kadu.
Tugevalt happelistes muldades, kus pH väärtus on alla 5,5 toimub enamasti ainult keemiline reaktsioon – oksüdeerunud lämmastikühendite taandamine.
Molekulaarne N2 moodustub keemilisel teel lämmastikhappe ja aminohapete või ammooniumsoolade vahel pH väärtusel alla 5,5.
Kui lähetume mikrobioloogilistest protsessidest, siis protsessi, mil molekulaarne lämmastik tekib keemiliste reaktsioonide tulemusel, nimetatakse kaudseks denitrifikatsiooniks.
Põhiliseks oksüdeerunud lämmastikühendite taandamisprotsessiks, mille tulemusel tekib lämmastiku kadu mullas, on mikrobioloogilised protsessid ehk otsene denitrifikatsioon. Siis kasutavad bakterid molekulaarse O2 asemel nitraatide hapnikku ja lämmastik redutseeritakse kuni molekulaarse vormini.
Peamisteks nitrifikaatoriteks mullas on Pseudomonas aeruginosa, Pseudomonas denitrificans, Micrococcus denitrificans jt. Denitrifikatsiooni võivad põhjustada ka väävlibakterid (nt Thiobacillus denitrificans). Sel juhul on energiaallikaks kas molekulaarne väävel või tiosulfaat, mis muudetakse sulfaadiks. Samas nitraat taandatakse kuni gaasilise lämmastikuni.
Kui lähetume mikrobioloogilistest protsessidest, siis protsessi, mil molekulaarne lämmastik tekib keemiliste reaktsioonide tulemusel, nimetatakse kaudseks denitrifikatsiooniks.
Põhiliseks oksüdeerunud lämmastikühendite taandamisprotsessiks, mille tulemusel tekib lämmastiku kadu mullas, on mikrobioloogilised protsessid ehk otsene denitrifikatsioon. Siis kasutavad bakterid molekulaarse O2 asemel nitraatide hapnikku ja lämmastik redutseeritakse kuni molekulaarse vormini.
Peamisteks nitrifikaatoriteks mullas on Pseudomonas aeruginosa, Pseudomonas denitrificans, Micrococcus denitrificans jt. Denitrifikatsiooni võivad põhjustada ka väävlibakterid (nt Thiobacillus denitrificans). Sel juhul on energiaallikaks kas molekulaarne väävel või tiosulfaat, mis muudetakse sulfaadiks. Samas nitraat taandatakse kuni gaasilise lämmastikuni.
Foto 1. Allikas: http://web.mst.edu/~microbio/BIO221_2009/P_aeruginosa.html
Denitrifikaatorid on fakultatiivesed anaeroobid ja nitraate kasutavad nad põhiliselt O2 puudumisel. Seega denitrifikaatorid kasvavad aeroobselt ilma nitraatideta või anaeroobselt nende olemasolul.
Ligikaudu 70% lämmastikväetistest kasutavad taimed. Osa kadudest tekib sademetega välja uhtumisel, teise osa tekitavad mikrobioloogilised jt. protsessid.
Denitrifikatsioon on suurem looduslikes, happelistes ja paakunud muldades võrreldes kultuurmuldadega.
Õhulämmastiku sidumine
Looduses on mikroorganisme, mis võivad omastada molekulaarset lämmastikku ja sünteesida sellest oma rakus kõik vajalikud lämmastikku sisaldavad orgaanilised ühendid. Nad esinevad keskkonnas kas vabalt või sümbioosis kõrgemate organismidega, näiteks: taimedega.
19. sajandi lõpul leiti, et õhulämmastikku võivad siduda nii mullas vabalt elavad kui ka taimedega sümbioosis elavad ja mügaraid moodustavad bakterid.
Mullas vabalt esinevad õhulämmastikku siduvate bakterite hulka kuulub näiteks Clostriduim spp. Nad on anaeroobsed, peritrihhaalse viburite asetusega pulgakujulised bakterid, kes võivad moodustada endospoore Õhuhapniku olemasolul võivad nad paljuneda siis, kui keskkonnas esineb aeroobseid hapnikku siduvaid baktereid. Clostridium pasteurianum`it, nagu kas teisi liike (Clostridium butyricum, Clostridium acebutyricum, Clostridium pectinoforum, Clostridium felsineum), võib esineda nii happelises (pH 4,5 – 5,5) kui ka leeliselises (ph 8,0 – 9,0) keskkonnas. Resistentsed välistingimuste suhtes on eriti nende (endo-)spoorid.
Lämmastiku allikana võivad Clostridium`i perekonda kuuluvad liigid kasutada nii ammooniumsoolasid kui ka mitmeid lämmastikku sisaldavaid orgaanilisi ühendeid ning nende puudusel omastada ka molekulaarset lämmastikku. Paljunedes keskkonnas, mis sisaldab kas mono-, di- või mitmeid polüsahhariide (dekstriin, tärklis), saavad nad energiat, produtseerides keskkonda- ja äädikhapet, süsihappegaasi ning vesinikku.
Clostridium spp. peetakse vähese aktiivsusega õhulämmastiku sidujateks. Tema aktiivsuse piiriks loetakse 1 – 3 mg lämmastikku 1 g kääritatava energeetilise materjali kohta.
Aktiivsemateks õhulämmastiku sidujateks mullas on aeroobsed asotobakterid(Azotobacter chroococcum, Azotobacter vinelandii, Azotobacter aglis jt). Nad on polümorfsed ja seotud lämmastiku (nitritite, nitraatide, aminohapete jt.) puudumisel omastavad õhulämmastikku. Osa seotud lämmastikust eritatakse eksosmoosil ümbritsevasse keskkonda kas amiinohapetena või ammoniaagina. Energeetilise materjalina võivad nad kasutada nii mono-, di- kui ka mõningaid teisi polüsahhariide ja mitmeid alkohole, orgaanilisi happeid, sh. ka aromaatseid (näiteks bensoehape). Nad ei kasuta tselluloosi, kuid tselluloosirikas materjal (põhk, põhurikas sõnnik) intensiivistab nende paljunemist. Põhjendatav on see sellega, et tselluloos lõhustatakse mullas tsellulolüütiliste bakterite (Cellvibrio spp., Cellulomonas spp., Cellfalcicula spp. jt) poolt lihtsamateks süsivesikuteks, mida saavad kasutada asotobakterid.
Azobacter spp. leidub enamuses neutraalse pH-ga mullas, kuid troopilistest muldadest on leitud ka happeresistentseid liike. Asotobakterite õhulämmastiku sidumisvõime kõigub suurtes piirides 5 – 20 mg 1 g energeetilise materjali kohta.
Peale eeltoodu võib mullast leida veel teisigi õhulämmastikusidujaid, nt Pseudomonadacae, Spirilacaeae, Achromobacteriaceae, Eneromobacteriaceae, Bacillaceae ja Mycobacteriaceae sugukondadest. Õhulämmastiku sidumisvõime on ka mitmetel sini-rohevetikatel.
Ligikaudu 70% lämmastikväetistest kasutavad taimed. Osa kadudest tekib sademetega välja uhtumisel, teise osa tekitavad mikrobioloogilised jt. protsessid.
Denitrifikatsioon on suurem looduslikes, happelistes ja paakunud muldades võrreldes kultuurmuldadega.
Õhulämmastiku sidumine
Looduses on mikroorganisme, mis võivad omastada molekulaarset lämmastikku ja sünteesida sellest oma rakus kõik vajalikud lämmastikku sisaldavad orgaanilised ühendid. Nad esinevad keskkonnas kas vabalt või sümbioosis kõrgemate organismidega, näiteks: taimedega.
19. sajandi lõpul leiti, et õhulämmastikku võivad siduda nii mullas vabalt elavad kui ka taimedega sümbioosis elavad ja mügaraid moodustavad bakterid.
Mullas vabalt esinevad õhulämmastikku siduvate bakterite hulka kuulub näiteks Clostriduim spp. Nad on anaeroobsed, peritrihhaalse viburite asetusega pulgakujulised bakterid, kes võivad moodustada endospoore Õhuhapniku olemasolul võivad nad paljuneda siis, kui keskkonnas esineb aeroobseid hapnikku siduvaid baktereid. Clostridium pasteurianum`it, nagu kas teisi liike (Clostridium butyricum, Clostridium acebutyricum, Clostridium pectinoforum, Clostridium felsineum), võib esineda nii happelises (pH 4,5 – 5,5) kui ka leeliselises (ph 8,0 – 9,0) keskkonnas. Resistentsed välistingimuste suhtes on eriti nende (endo-)spoorid.
Lämmastiku allikana võivad Clostridium`i perekonda kuuluvad liigid kasutada nii ammooniumsoolasid kui ka mitmeid lämmastikku sisaldavaid orgaanilisi ühendeid ning nende puudusel omastada ka molekulaarset lämmastikku. Paljunedes keskkonnas, mis sisaldab kas mono-, di- või mitmeid polüsahhariide (dekstriin, tärklis), saavad nad energiat, produtseerides keskkonda- ja äädikhapet, süsihappegaasi ning vesinikku.
Clostridium spp. peetakse vähese aktiivsusega õhulämmastiku sidujateks. Tema aktiivsuse piiriks loetakse 1 – 3 mg lämmastikku 1 g kääritatava energeetilise materjali kohta.
Aktiivsemateks õhulämmastiku sidujateks mullas on aeroobsed asotobakterid(Azotobacter chroococcum, Azotobacter vinelandii, Azotobacter aglis jt). Nad on polümorfsed ja seotud lämmastiku (nitritite, nitraatide, aminohapete jt.) puudumisel omastavad õhulämmastikku. Osa seotud lämmastikust eritatakse eksosmoosil ümbritsevasse keskkonda kas amiinohapetena või ammoniaagina. Energeetilise materjalina võivad nad kasutada nii mono-, di- kui ka mõningaid teisi polüsahhariide ja mitmeid alkohole, orgaanilisi happeid, sh. ka aromaatseid (näiteks bensoehape). Nad ei kasuta tselluloosi, kuid tselluloosirikas materjal (põhk, põhurikas sõnnik) intensiivistab nende paljunemist. Põhjendatav on see sellega, et tselluloos lõhustatakse mullas tsellulolüütiliste bakterite (Cellvibrio spp., Cellulomonas spp., Cellfalcicula spp. jt) poolt lihtsamateks süsivesikuteks, mida saavad kasutada asotobakterid.
Azobacter spp. leidub enamuses neutraalse pH-ga mullas, kuid troopilistest muldadest on leitud ka happeresistentseid liike. Asotobakterite õhulämmastiku sidumisvõime kõigub suurtes piirides 5 – 20 mg 1 g energeetilise materjali kohta.
Peale eeltoodu võib mullast leida veel teisigi õhulämmastikusidujaid, nt Pseudomonadacae, Spirilacaeae, Achromobacteriaceae, Eneromobacteriaceae, Bacillaceae ja Mycobacteriaceae sugukondadest. Õhulämmastiku sidumisvõime on ka mitmetel sini-rohevetikatel.